ИЗ ИСТОРИИ МОЛЕКУЛЯРНОЙ ФИЗИКИ.
А.И. НАДЕЖДИН (1858-1886)
Опубликовано в сборнике
«Исследования по истории физики и механики», М., Наука, 1990, стр. 5-36.
СОДЕРЖАНИЕ:
Три четверти жизни
Киевская физическая лаборатория
Начало научной деятельности
«Стипендиат без пособия»
Естественно-научные взгляды
Критические явления
Давление насыщенного пара
Термодинамическое подобие
Модели в термодинамике и строение жидкостей
Мотивы научного творчества
Примечания.
[Ссылки на примечания в тексте показаны в круглых скобках, напр. (1)].
Приложение 1. А. И. Надеждин: Экспериментальное и теоретическое исследование изменения агрегатного состояния тел.
Приложение 2. Н. Н. Шиллер: План предполагаемых занятий г. Надеждина во время его заграничной командировки.
Литература
[Ссылки на литературу и архивные материалы показаны в квадратных скобках]
Имя русского физика Александра Ивановича Надеждина вошло в энциклопедии, упоминается оно и в историко-научной литературе. Однако его яркая личность и беспрецедентная по мощности работа заслуживает того, чтобы посвятить ему специальную статью, тем более что в творчестве Надеждина отразился короткий, но важный этап развития молекулярной физики. Кроме того, для нас небезразличны детали тогдашней академической жизни, сохранившиеся лишь в архивных документах.
В статье использованы все сочинения Надеждина [1— 20], опубликованные биографические сведения о нем [21, 22], а также ряд архивных и малодоступных материалов, источники, передающие научную и академическую атмосферу эпохи.
1.ТРИ ЧЕТВЕРТИ ЖИЗНИ
Биография молодого человека, целиком отдавшегося науке и не дожившего до 28 лет, не может быть длинной, но она по-своему интересна. В Киевском городском архиве хранится выписка Курской духовной консистории из метрической книги "Обоянского уезда села Михайловского, Верхопенье тож Архангельской церкви 1858 г.”; в ней значится 19 июня рождение, а 25-го крещение Надеждина Александра, родители коего суть: ”Конно-артиллерийской ополченской батареи доктор Коллежский Асессор Иван Афанасьевич Надеждин и законная жена его Ольга Петрова” [23, л. 24].
Отец А. И. Надеждина [Там же, л. 22—46] родился в 1823 г., в 1847 г. окончил Медико-хнрургическую академию в Петербурге "казенным студентом” и с тех пор вел кочевую жизнь военного врача; он не раз "находился в походах" в действующей армии, начиная с "войны в союзе с Австрийскою Армиею» против мятежных Венгров" (1849) [Там же, л. 28] и кончая русско-турецкой войной (1877-1878), когда он был уже главным врачом полевого госпиталя [21, с. VIII]. ”В воздаяние отличия, оказанного в сражении с турками 24 июля 1854 г.” и ”за подавание помощи раненым под выстрелами неприятеля во время боя под Карсом” [23, л.29об., 32об.] был дважды "всемилостивейше пожалован” суммами по 125 руб. 47 коп.
В 1857 г. И.А. Надеждин женился на ”дочери умершего подпоручика Протопопова, девице Ольге Петровой”, сестра которой Александра Петровна Протопопова, владелица упомянутого Верхопенья, и помогла поднять первенца в первый год его жизни.
Детство мальчика прошло в переездах с родителями, пока наконец в 1870 г. семья не осела в Киеве, где отец получил место старшего ординатора Киевского военного госпиталя и вскоре купил домик неподалеку от госпиталя на Рыбальской улице (этот район Киева в юго-западной части города назывался Печерском).
Сына же он определил во второй класс 1-й Киевской гимназии. По свидетельству Б.Я. Букреева, товарища (и биографа) Надеждина, ”из всех предметов гимназического курса литература всего более приходилась ему по душе, и ею он занимался с наибольшей охотой и успехом; что же касается физики, которая впоследствии сделалась его излюбленным предметом, то, к удивлению, в ней он успевал сравнительно менее, хотя наклонность к различным механическим занятиям замечалась в мальчике уже с самых ранних лет. Дома он устроил себе целую химическую лабораторию и таким образом еще в гимназии приобрел значительный запас сведений по химии” [21, с. VIII].
27 июня 1877 г. А.И. Надеждину был выдан аттестат зрелости, из которого можно узнать, что ”на основании наблюдений за все время обучения его в Киевской 1-й гимназии поведение его было вообще отличное, исправность в посещении и приготовлении уроков, а также в исполнении письменных работ отличные, прилежание отличное и любознательность вообще ко всем предметам весьма удовлетворительная”. В двух столбцах отметок — "выставленных в Педагогическом совете” и "выставленных на испытании” (которое представляло серию из 12 экзаменов) — почти сплошь "отлично”, и лишь по физике и математической географии "хорошо”. ”Во внимание к постоянно отличному поведению, прилежанию и к отличным успехам в науках Александр Надеждин ... удостоен награждения золотой медалью” [23, л. 21-21об.].
Аттестат давал право поступления в университет; "Александр Надеждин ... 19 лет от роду, телосложения крепкого” [Там же, л. 26], записывается на математическое отделение физико-математического факультета.
Вероятно, после жестко регламентированной гимназической жизни взяла свое потребность в вольном развитии. "Лекции своего факультета он посещал далеко не все, часто ходил на лекции других факультетов, дома много читал, а еще больше занимался различными физическими и химическими опытами, сам устраивал себе приборы и т.д.” [21, с. VIII— IX]. Свои студенческие годы Надеждин прожил в два этапа. После первых двух курсов он воспользовался возможностью отправиться за границу "в качестве репетитора детей одного богатого русского семейства” [Там же, с. VIII]. С опозданием, по-видимому, уже перед самым отъездом, он успел сдать экзамены за четыре семестра (1) , сжигать корабли он не собирался.
Долгое отсутствие (Надеждин пропускал 1879/80 учебный год) влекло за собой отчисление из университета, и все же игра стоила свеч: пять месяцев, полные новых разнообразных впечатлений, — от средиземноморской природы в Ницце до лекций К. Фламмариона в Париже, — дали очень много для развития талантливого молодого человека, в частности для овладения иностранными языками (в гимназии было два древних языка, а из новых — лишь французский).
Возвратившись в Киев, путешественник вновь записывается в студенты, уже на третий курс (с 1 сентября 1880 г.). Отсюда и нужно отсчитывать начало собственно научной работы А.И. Надеждина, а именно – работы в Физической лаборатории университета.
2. КИЕВСКАЯ ФИЗИЧЕСКАЯ ЛАБОРАТОРИЯ
В этом месте требуется краткое отступление. Физика в Киевском университете возглавлялась в это время М. П. Авенариусом — серьезным ученым, заботливым учителем и глубоко порядочным и хорошим человеком [25-27]. С 1875 г. к нему в помощь пришел ученик А.Г. Столетова, талантливый теоретик Н.Н. Шиллер (для которого вскоре была учреждена и кафедра). Еще до того хлопотами Авенариуса несколько улучшилась и материальная база. Помимо "физического кабинета” (аудитории площадью около 200 кв. м и хранилища приборов для демонстрации), „с 1874 г. существует при университете и Физическая лаборатория, — засвидетельствовал Авенариус в 1884 г., — на устройство ее, т.е. на приобретение необходимых приборов, университет пожертвовал из своих специальных средств тогда же 2000 р. А затем на эту лабораторию никаких сумм не отпускалось, и она пользовалась приборами физического кабинета. Работали в лаборатории студенты физико-математического факультета разряда математических наук, некоторые уже окончившие университет молодые ученые, консерватор кабинета и профессора физики” [28, с. 81].
"Выдающаяся научная деятельность киевской физической лаборатории” [27, с. 422], посвященная экспериментальному изучению жидкостей при высоких температурах, включая критическую, широко известна [29—33]. Деятельность эта началась с собственных исследований Авенариуса по критическим явлениям (1873), а с 1875 г., после того как рабочее помещение несколько увеличилось, в нее включились первые его ученики и сотрудники – В. И. Зайончевский (2), затем К. Н. Жук (3), а в течение 1880 г. О. Э. Страус(4).
К 80-м годам прошлого века работы лаборатории приобрели европейскую известность; достаточно сказать, что данные Зайончевского (Авенариус назвал их "классическими” [43]) послужили экспериментальной основой в установлении принципа соответственных состояний (Ван-дер-Ваальс, 1880).
В 1879 г. Авенариус уже решается предложить свою проблематику как "тему сочинения для соискания студентами наград медалями”; тема называлась ”Об изменениях, замечаемых в свойствах тел вблизи так называемой температуры абсолютного кипения” [44]. (Едва ли нужно напоминать, что термин принадлежит Д.И. Менделееву, однако после исследований Т. Эндрюса он был вытеснен современным — критическая температура.)
В разборе представленных работ М.П. Авенариус разъяснял: "Предложил я для соискания наград именно эту тему ввиду того, что имеющиеся у нас в физическом кабинете приспособления дают возможность и студентам в случае приложения ими достаточных стараний получить по названному вопросу такие результаты опытов, которые имели бы положительный научный интерес” [43, л. 6]. "Приспособления”, о которых говорит здесь Авенариус, кажутся сейчас простыми и даже наивными: воздушные термостаты — вставленные друг в друга металлические ящики с наружным нагревом (это устройство было изобретено одним из учителей Авенариуса, Г. Магнусом в 1842 г. [45]), газовые горелки, стеклянные трубки. Суть измерений заключалась в фиксации объема жидкости и давления пара при каждой температуре по мере нагревания и в наблюдении температуры, при которой исчезает мениск. При более близком рассмотрении эта экспериментальная техника, вышедшая из употребления уже в начале нашего века, оказывается отнюдь не столь примитивной. И поддержание постоянной температуры (в лаборатории пользовались для этого четырьмя последовательно вставленными друг в друга ваннами — ведь не было ни электромоторов, ни соответственно вентиляторов-мешалок), и ее измерение в разных зонах воздушными и ртутными термометрами, и определение емкости рабочей части трубки, и монтаж придуманного Зайончевским горизонтального манометра – все это держалось на множестве остроумных приемов и вместе с тем требовало большого мастерства и аккуратности, прекрасного владения стеклодувной горелкой, громадного терпения и… крепких нервов, ибо трубки под давлением часто взрываются.
Впоследствии как раз Надеждин составил подробное описание техники эксперимента, которая была принята в Киевской лаборатории (и в которую сам он внес немало усовершенствований). Это описание [11, с. 54—74] и ныне читается почти как роман.
3. НАЧАЛО НАУЧНОЙ ДЕЯТЕЛЬНОСТИ
Вот здесь-то, среди ’’магнусовых ванн” и газовых горелок, и дебютировал Надеждин-ученый.
Поставленная конкурсная тема стала для него вызовом: критическое состояние пребывало на острие интересов тогдашней физики (5), так что новизна предмета обязательно должна была привлечь жадную любознательность молодого человека.
Вместе с Надеждиным еще несколько студентов пробовали свои силы. Из четырех представленных сочинений, писал Авенариус, ’’три вполне оправдали мои ожидания”, причем на экспериментальную часть работы каждый из авторов ’’потратил около 1/2 года постоянных занятий в физической лаборатории” [43, л.6]. Коллегами Надеждина, до конца прошедшими первый этап научного марафона, были студенты Дм. Дьячевский и И. Каннегисер; они получили данные по расширению жидкостей при высоких температурах, которые были затем обработаны К.Н. Жуком и опубликованы им в 1884 г. [47], но больше в физической лаборатории не работали. (Оба окончили университет кандидатами в 1881 г.)
Для Надеждина же это было только начало. Из отзыва на его сочинение, составленного Авенариусом: ’’Обращая внимание на обстоятельное изложение всего вопроса <...> в особенности же на прекрасно произведенные опыты над упругостями паров двух жидкостей вплоть до предельной температуры их существования, которые, — после классических работ Зайончевского, — представляют единственные данные в этом отношении, считаю это рассуждение заслуживающим золотой медали” [43, л. 7].
Медаль Надеждин получил, равно как и так называемую Пироговскую премию — 100 руб. (Тут уже была доля везения: премию разыгрывали по жребию между медалистами двух отделений факультета [48]). Солидная по тем временам сумма была очень кстати Надеждину, тратившему заметные средства на домашние опыты. Его интересовали все физические новинки. Он собственноручно строил у себя дома телефоны, микрофоны, аккумуляторы, и нередко эти приборы служили для демонстрации на лекциях профессора [22].
И все же не одна физика поглощала молодого человека, Он занимался философией – перевел главу о Канте в русском издании ’’Истории европейской философии” А. Вебера, 1882 – (6) , записался в члены-любители Драматического кружка, занимался он также музыкой и среди друзей был известен как прекрасный пианист. Кроме того, он принимал "самое горячее участие, словом и делом, в Киевских народных чтениях”; он там читал лекции большей частью по метеорологии (в университете эту дисциплину вел Авенариус), относился к ним ”с большим увлечением и часто тратил массу времени на то, чтобы привести необходимые приборы в такое состояние, при котором можно было рассчитывать на удачные опыты” [21, с. IX].
В мае 1882 г. Надеждин закончил выпускные экзамены. Из 25 предметов, перечисленных в выпускной ведомости, 10 было сдано еще в 1879 г., оставались главным образом механико-математические дисциплины (7), которые были сданы на круглые пятерки (только геодезия на четверку) [49]. Ранее, 22 и 29 февраля 1882 г., состоялись письменные испытания на соискание кандидатской степени. Первый из вопросов был: "Экспериментальное и теоретическое исследование изменения агрегатного состояния тел”, второй — "Сравнение электромагнитной и электрической единиц количества электричества” (Оба вопроса записаны рукой Авенариуса). Оба экзаменационные сочинения сохранились [50, приложение 1; 51]. Спору нет, ни в одном из них не содержится нового материала, но сам уровень изложения, равно как и круг рассмотренных вопросов и использованной литературы, достаточно поучительны. В особенности это относится к первому, так сказать, профилирующему сочинению. Так, например, рассуждения о термодинамической поверхности, тройной точке (названной "второй критической точкой” — терминология тогда еще не установилась) и о возможности критических переходов жидкость—твердое тело отражают знакомство с первыми статьями Дж.У. Гиббса (Надеждин и пользуется гиббсовыми обозначениями) и с новейшим сочинением М. Планка [52].
А многим ли в европейской науке были известны труды Гиббса к началу 1882 г.? Еще любопытный штрих: номер "Анналов” Видемана со статьей Планка [52] вышел в свет 15 февраля 1882 г., а меньше чем через три недели (22 февраля ст. ст.) эта статья уже освоена Надеждиным.
Итак, студенческая пора осталась позади, говоря словами канцелярского документа, "Надеждин Александр окончил курс наук на физико-математическом факультете Университета Св.Владимира по отделению математических наук к 1 июня 1882 года и по выдержании установленного испытания физико-математическим факультетом удостоен степени кандидата математических наук и в этой степени Советом Университета Св.Владимира утвержден в заседании 31 мая 1882 г.” [53, л. 14],
4. «СТИПЕНДИАТ БЕЗ ПОСОБИЯ»
Блестящее окончание университета обеспечило Надеждину избрание стипендиатом для приготовления к профессорскому званию, причем "наблюдение за его занятиями факультет поручил проф. М.П. Авенариусу и Н.Н. Шиллеру” [23, л. 5]. Извещение об утверждении Надеждина стипендиатом (на первый год, с 31 мая 1882 г. по 31 мая 1883 г.) адресовано, в частности, г. библиотекарю — ”для продолжения выдачи книг из библиотеки Университета г. Надеждину” [54, л.146,195].
От современной очной аспирантуры при кафедре случай Надеждина отличался не только сроком, но и финансовым обеспечением. Как говорилось в записке декана, "факультет не может оказать г. Надеждину поддержки в дальнейших его ученых занятиях, так как все стипендии для приготовления к профессорскому званию в настоящее время замещены и не скоро будут свободны” [23, л.1]. Поэтому молодой ученый стал "стипендиатом без пособия” [Там же, л. 5].
С сентября 1882 г. факультет начал хлопоты о предоставлении необходимых средств (600 руб. в год). Однако время для таких хлопот выпало неудачное. Надо вспомнить, что прошло немногим больше года со времени убийства народовольцами Александра II, и ужесточение во всех сферах жизни быстро набирало силу. Реакционный университетский устав 1884 г. еще только лишь вынашивался (8), но линия на всяческие ограничения уже явственно пролегла от министерства народного просвещения к учебным округам. В ответ на ходатайство Киевского учебного округа министерство затребовало (письмо от 18 января 1883 г.) подробные сведения о Надеждине: "какие он оказал успехи в науках или сделал опыты в научных трудах, о его дарованиях, предварительном образовании (где и с каким успехом окончил гимназический курс, чем и как занимался в Университете и какие сочинения изучал и т.д.), а также более или менее подробную характеристику личности Александра Надеждина” [23, л. 8, 8 об.]. Декан физико-математического факультета Н.А. Бунге собственноручно пишет хвалебную характеристику своему подопечному, подчеркивая, в частности, что Надеждин — "сын статского советника”, что за границу он уезжал ”с семейством, мне лично известным с самой лучшей стороны”, и что без пособия "ему будет трудно продолжать свои научные занятия, начатые с таким успехом” [Там же, л. 10,10 об]. После этого, уже в марте 1883 г., следует разрешение министра на стипендию Надеждину — но сроком лишь на один год (9). Поэтому с марта 1884 г. начинается переписка о продлении стипендии еще на один год. Министерство первоначально отказывает, но после повторного ходатайства университета, уже в осеннем семестре, дает согласие на уплату стипендии "в текущем полугодии”.
Эта переписка тянулась, казалось, бесконечно, а выпускник университета должен был обеспечить себе заработок. С осени 1882 г. в течение двух лет Надеждин преподает математику и космографию в Киевской женской гимназии. Подобное совместительство в те времена было правилом, а не исключением. Так, Зайончевский преподавал в этой же гимназии, Жук — в 3-й Киевской, Шиллер — в военной гимназии (1876—1881). Вкладывая душу в любое дело, за которое брался, новый учитель быстро завоевывает репутацию "хорошего преподавателя и блестящего лектора” [22]. На выпускном акте гимназии 15 июля 1883 г. он произносит интересную речь ”0 некоторых новейших исследованиях, в связи с общим направлением современной физики” [4]. Большая часть этой речи — обзор работ о передаче на расстояние сигналов, и в особенности изображений. Вообще, электричество очень занимало Надеждина, и одна из его последних работ посвящена испытанию элемента цинк-серная кислота-медь при добавке в раствор перманганата калия. Он проницательно заметил, что "огромная начальная сила элемента с марганцово-кислым кали <…> делает его годным для приведения в действие индуктивных приборов, взрыва мин и т.п.” [19, с.LI]. Быть может, Надеждин, проживи он дольше, обратился бы к электротехнике, подобно Страусу и Авенариусу. А пока он увлеченно работал в физической лаборатории, определял критические свойства жидкостей и усердно штудировал литературу.
В начале 1883 г. по рекомендации К.Н. Жука Надеждин был избран в Киевское общество естествоиспытателей [56]. Основанное в 1869 г. (среди членов-учредителей были М.П. Авенариус и В.И. Зайончевский) Общество согласно уставу имело цели:
”а) исследовать органическую и неорганическую природу <…> преимущественно в полосе России, граничной с губерниями Киевского учебного округа; б) способствовать развитию естественных наук вообще; в) распространять естественно-исторические знания в России” [57, с. 1]. Ко времени прихода Надеждина Общество насчитывало свыше ста членов, большей частью биологов и медиков, но также физиков, химиков и даже математиков. Здесь Надеждин нашел небольшую (обычно десятка полтора слушателей), но заинтересованную аудиторию, которой рассказывал о всех своих исследованиях, как о главных, тех, что вел в университете, так и о домашних.
”Вечно торопливый, вечно занятой, он как бы спешил жить <…>. Все его интересовало, все ему хотелось знать и испытать <...> во все, за что бы он ни принимался, он вкладывал всю свою душу, во всем старался достигнуть чего-нибудь существенного” [21, с. XII]. Эта "непомерная жажда работы” [Там же, с. XI], благодаря которой он и успевал невероятно много, имела, увы, оборотную сторону: здоровье молодого человека стало быстро сдавать. Надо думать, его "крепкое телосложение” было сломлено не столько количеством работы, сколько ее условиями.
В тесном помещении (высотой всего 2,4 м) "среди зажженных газовых горелок и накаленных жестяных магнусовских ванн, в невыносимо высокой температуре, в сухой, переполненной углекислотой атмосфере” [25, с. 52] каждый день часами находились и сам Авенариус, и его ученики. Но Надеждин работал на износ и, главное, имел дело со многими органическими жидкостями, в том числе хлорпроизводными, а потом и с бромом. Если осушивание и перегонку их можно еще было наладить, то сами измерения, при которых очень часто происходят взрывы, сделать безопасными было невозможно. Да и о предельно допустимых концентрациях тогда не думали.
В сентябре 1884 г. Надеждин подает ректору прошение о допущении к испытаниям на степень магистра физики [58]: в начале 1885 г. и устные и письменные экзамены (соответствующие нынешнему кандидатскому минимуму) были сданы, дело оставалось за диссертацией. Автор задумал ее как три связанные между собой очерка: "Расширение твердых тел”, ”О расширении жидкостей и переходе тел из жидкого состояния в газообразное”, ”Об упругости насыщенных паров”. С осени 1885 г. он начал публиковать диссертацию по главам в "Университетских известиях” под названием ”Этюды по сравнительной физике”. В марте 1886 г. "Этюды” вышли и отдельным изданием [10]. Во внешнем оформлении текста, особенно в ссылках на литературу, видны следы спешки. Легко понять, что Надеждин действительно торопился: силы его были на исходе.
Защита диссертации едва ли имела иное значение, кроме формального. По определению факультета "официальными оппонентами назначены проф. Авенариус и проф. Шиллер” [53]. Диспут состоялся 8 апреля 1886 г. в 1 час пополудни. "Работа была настолько выдающаяся, — вспоминал очевидец, — что оппонентам оставалось говорить почти только об ее достоинствах; единственный существенный упрек, который был сделан диспутанту, состоял в том, что в диссертацию не вошел оригинальный метод А. И-ча для определения критической температуры” [21, с. XI].
Не дожидаясь защиты, факультет уже в середине 1885 г. возбудил ходатайство "о командировании г. Надеждина за границу на два года на казенный счет” — "как для дальнейшего усовершенствования г. Надеждина в науках, так и для лучшего подготовления его к преподавательской деятельности” [59, л. 400]. Заграничная стажировка была естественным правилом научного образования и для России, и для стран Западной Европы.
В представлении, которое сделал Н.Н. Шиллер, содержался краткий обзор работ Надеждина и указывалось, что ”г. Надеждин, кроме изучения литературы и теоретической стороны предмета, неутомимо занимался экспериментальными упражнениями и исследованиями в физическом кабинете и, несмотря на бедность этого последнего, сумел достигнуть достойных внимания результатов <…> Факультет, командируя его за границу, может с уверенностью ожидать выработки из г. Надеждина солидного ученого и полезного преподавателя” [Там же, л. 402]. Вскоре Шиллер подготовил и программу занятий для Надеждина [60] (см. Приложение 2).
Разрешение на командировку последовало сравнительно быстро – всего лишь через семь месяцев. Вскоре после защиты, 6 мая, Надеждин выехал в Берлин. Он рассчитывал сначала восстановить силы после громадного напряжения предыдущих лет. Но было слишком поздно: здоровье его было полностью разрушено, попытка лечения в Францесбаде (Богемия) уже не помогла. 6 июня 1886 г. А.И. Надеждин скончался, не дожив двух недель до 28 лет. ”Тело его было перевезено в Киев и предано земле на Аскольдовой могиле” [21, с. XII].
Для увековечения памяти Надеждина главные его работы были изданы (на средства родителей) отдельной книгой [11]. Кроме того, вторая и третья части "Этюдов”, содержащие собственные данные автора, были опубликованы по-немецки в переводе Авенариуса [12,13].
Пропагандировал работы Надеждина также "Вестник опытной физики и элементарной математики”. Его редактор Э.К. Шпачинский договорился с Б.Б. Голицыным об обзоре новейших воззрений на жидкое и газообразное состояние (”эта работа была обещана для нашего журнала покойным моим приятелем А.И. Надеждиным”, — пояснял он). При этом он подчеркнул: ”в этом вопросе нельзя игнорировать работ Киевской физической лаборатории, а в особенности последних исследований того же Надеждина, а потому было бы более нежели странно в Киевском физ [ическом] журнале, воздавая должное заслугам в этой области van der Waals’а, вовсе умолчать о работах Надеждина” [61]. В большой статье Голицына [62] это пожелание выполнено (автор пользовался "Физическими исследованиями”, присланными ему Шпачинским [61]).
5. ЕСТЕСТВЕННО-НАУЧНЫЕ ВЗГЛЯДЫ
В качестве эпиграфа к научному творчеству Надеждина можно было бы взять девиз Г. Камерлинг-Оннеса: "Через измерения — к закономерностям” (В оригинале это звучит лучше: Door meten tot weten) . Этих слов Надеждин не знал (хотя работу Оннеса "Общая теория жидкостей” [63] цитировал). Но вот что писал Надеждин: "Изучение свойств физических, подверженных более или менее строгому измерению, может давать не только результаты качественные (каковы по большей части результаты физической химии), но и количественные, могущие служить основанием или проверкой математических дедукций” [11, с. 5]. Идейное родство с девизом Оннеса очевидно.
Ко времени, когда Надеждин пришел в физику, все естествознание развивалось под девизом единства природы, "единства физических сил” (название знаменитой книги А. Секки). Установление закона сохранения энергии и возникновение термодинамики (10) , открытие периодического закона, укрепившее древнее представление о единстве вещества, становление атомно-молекулярного учения в химии и возникновение "кинетической теории материи” — таковы великие события, создавшие научную атмосферу, которой дышал Надеждин.
Вот сжатая оценка состояния физики, данная русским физиком Н.А. Гезехусом в 1882 г.: "Стремления современных ученых — проникнуть вглубь, в сущность изучаемого предмета, обобщить, связать между собою наблюдаемые явления и свести их окончательно к механическим принципам. Все внимание устремлено на молекулярные движения, на внутренние силы. Пришлось даже ввести новый отдел науки — физику частичных сил, одно название которого характеризует господствующее направление новейших исследований. С особым тщанием изучаются свойства газов и создается кинетическая теория газов. Выдвигается всеобъемлющая механическая теория теплоты и, наконец, делаются уже серьезные попытки основать и механическую теорию электричества” [64, с. 533].
Конечно, и для Надеждина ”усилия нынешней физики <...> установить механическое объяснение всех естественных явлений” — "безусловная логическая необходимость” [4, с. 26, 27]. Здесь он нисколько не оригинален; иной, не механистической идеологии у естествознания просто не существовало. Однако оценка места и роли той области физики, которой он занялся, имеет уже и индивидуальный отпечаток.
”Изо всей физики наибольшей устойчивостью теории в связи с значительным количеством опытного материала обладает механическая теория тепла” [11, с. 5]. Но эта часть физики привлекательна для ученого не только и не столько своей надежностью. Для Надеждина очень важно, что она может быть связана больше, чем какой-либо другой раздел физики, с атомно-молекулярным учением, с представлениями о строении тел.
Дело в том, что стремление постичь молекулярные движения отнюдь не было всеобщим — успехи термодинамики порождали и противоположную тенденцию. Столетов писал, что "способ верно рассуждать о явлении, не покушаясь составить его отчетливый, но гадательный рисунок, представляет методологическую новость, которая выгодно оттеняет весь дальнейший ход науки” [65, с. 311].
Надеждин в этой обстановке избрал наиболее точную позицию — опираясь на несомненные законы термодинамики, не ограничиваться ими, но комбинировать их с дополнительными сведениями, с той или иной моделью: ”для приложения этих законов в различных частных случаях необходимы более определенные представления как о строении тел, так и о характере самих движений ” [11, с. 6]. Основа этих представлений о строении тел для Надеждина — атомизм. "Между тем как в химии атомистическая гипотеза получила такую степень вероятности, что позволяет химический атом считать реальностью, в физике существуют целые отделы, где строение материи предполагается непрерывным, вводится новое вещество с выходящими из ряда обыкновенных свойствами и т.п. Только этой неопределенности и шаткости можно приписать нападки последнего времени (Dellinsgausen’а [Dellinghausen – А.К.] и Stallo) на самую атомистическую гипотезу. Но раз изучение тепла, по распространенным воззрениям, стало изучением частичного движения, существование того, что движется, — мельчайших частиц, атомов, должно было сделаться вне всякого сомнения” [Там же].
Можно, конечно, заметить, что в среде, воспитавшей молодого ученого, эти высказывания звучали естественно. Вдобавок Н. Деллингсхаузен и Л. Б. Сталло, антиатомисты, которых упоминает Надеждин, профессиональными физиками не были (11). Дилетанты (хотя и в высоком смысле слова), они по рождению и по образованию принадлежали к эпохе, когда в науке еще царили "ложные притязания всем завладевшей философии” [66, с. 31], и занимались физикой, так сказать, умозрительно. Но это замечание было бы слишком поверхностно. Во-первых, критика даже и со стороны дилетантов, особенно Сталло, была достаточно серьезной (12). А во-вторых, и в "настоящей” физике в это время единодушия не было. Среди западноевропейских физиков, пожалуй, лишь один И. Д. Ван-дер-Ваальс был твердо убежден в реальности атомов и молекул как физических тел, тогда как Дж.К. Максвелл и Р. Клаузиус были более осторожны [71, с. 50] ,а ровесник Надеждина М. Планк предсказывал в 1882 г., что, "несмотря на большие прежние успехи атомистической теории, в конце концов все же придется снова ее оставить и решиться на принятие непрерывной материи” [52, с. 475].
Поэтому атомистическое сгеdо Надеждина более весомо и значительно, чем могло бы показаться на первый взгляд. И оно непосредственно связывает научные интересы Надеждина с учением о теплоте, ибо "ближайшее изучение строения тел явилось необходимым условием изучения теории тепла” [11, с. 6]. Цитированные слова взяты у Рауля Пикте [72, с. 18], но оброненное вскользь замечание Надеждин поднял до общей идейной основы своей конкретной научной работы, т.е. исследований тепловых свойств веществ.
И, наконец, последнее из общих замечаний. Надеждин наверняка не думал о прикладном значении своих исследований. Однако в историческом плане совершенно очевидно, что изучение тепловых свойств веществ поддерживалось, хотя и опосредованно и даже не всегда осознанно, но непрерывно, практическими потребностями ”века пара”. Киевский химик Г. М. Фонберг писал: ”В прежние времена, чтобы сделать полезное открытие, нужно было перешагнуть Науку, выйти из пределов ее, и этот шаг был всегда случайным или в человеке, его сделавшем, предзнаменовал гения. Ныне требуется для этого одно знание Науки и действительных нужд Техники” [73, с. 90].
6. КРИТИЧЕСКИЕ ЯВЛЕНИЯ
В историю науки Надеждин вошел прежде всего как исследователь критических явлений, по оценке Столетова [74, с. 14] "глубокий знаток” этого предмета.
Ранняя история изучения критических явлений может быть представлена последовательностью имен: Ш. Каньяр де Латур, М. Фарадей, Д.И. Менделеев, Т. Эндрюс, И.Д. Ван-дер-Ваальс. Именем Надеждина этот список завершается: идейно его работы принадлежат именно этому этапу развития учения о критических явлениях и вместе с тем открывают собой начало следующего этапа. Действительно, после того как понятие критического состояния окончательно установилось в трудах Эндрюса и Ван-дер-Ваальса, обнаружился небывалый, чрезвычайно острый дефицит фактических данных об этом состоянии. Накопление и осмысление экспериментальных данных потребовало около четверти века, и вклад Надеждина в этот процесс совершенно уникален.
Одна из его крупных заслуг здесь, как давно признано [29-32], — описание критической опалесценции. ("До сего дня критическая опалесценция – это одно из наиболее ярких проявлений критической точки” [75, с. 33].)
Правда, в классической статье Эндрюса было уже отмечено "характерное явление полос, перебегающих или волнующихся по всей его [вещества] массе” [76, с. 19, 36]. "Помутнение” отмечал и Авенариус [77], но подробное рассмотрение "характеристической мути” как существенного признака критического состояния впервые дал именно Надеждин. Соответствующее место из "Этюдов” заслуживает того, чтобы привести его еще раз хотя бы в отрывках (первый раз это сделал Столетов в 1892 г. [74]):
"Уничтожение раздела между паром и жидкостью где-нибудь посредине трубки сопровождается следующими явлениями: за несколько времени до исчезновения мениска жидкость начинает сильно кипеть, но скоро густая муть от пузырьков заменяется родом тумана, в жидкости и вне ее проявляются быстро двигающиеся струйки, и наконец раздел делается незаметным”. При обратном переходе "вначале посредине трубки появляется легкая муть (голубоватая в отраженном свете и желтоватая в пропущенном); муть эта темнеет, делается опаловой, затем молочно-белой; трубка становится непрозрачной, и наконец появляется сильно кипящая жидкость”. Надеждин описывает также явления, происходящие при неравномерном нагревании трубки по ее длине ("поэтому особенно важным является соблюдение обратного перехода пара в жидкость при медленном охлаждении”), а также случаи, когда взятое количество жидкости больше либо меньше, чем нужно для достижения критического состояния, и заключает: "нормальному критическому объему будут соответствовать появление и исчезновение мениска где-нибудь посредине трубки, а не вблизи ее концов, и густая интенсивная муть разом по всей длине трубки, сопровождающая обратный переход” (цит. по: [11, с. 67-68]).
Наблюдения Надеждина могли бы иметь двоякое значение — как фактическая основа для теоретического анализа критической опалесценции и как основа для определения критических параметров оптическими способами. К сожалению, своевременно его наблюдения не получили достаточной известности. Повторные описания критической опалесценции в 1893 и 1894 гг. [78,79] (на которые потом ссылался и М. Смолуховский ) были отнюдь не более точными, и лишь много лет спустя (в 1911 г.) заслуга Надеждина была отмечена в монографии Г. Камерлинг-Оннеса и В. Кезома [80, § 50].
Однако "момент характеристической мути” [17] стал прекрасным признаком критической точки при работе оптическим методом. Надеждин широко использовал этот метод. Но последний не всегда применим: если жидкость непрозрачна (бром) или воздействует на стекло (вода), наблюдать и критическую опалесценцию, и исчезновение мениска просто невозможно. Трудность казалась непреодолимой. И все же решение было найдено, красивое и неожиданное. Суть его такова. Пусть стеклянная или металлическая трубочка устанавливается на подставке, подобно коромыслу весов: если в такую трубку, уравновешенную пустою, ввести некоторое количество жидкости и запаять, то трубка наклонится; если затем трубку постепенно нагревать, то ”все время, пока жидкость будет тяжелее пара, конец с жидкостью будет всегда отклонен; в момент же критической температуры и дальше — трубочка, как наполненная однородным веществом, будет находиться в равновесии. Если теперь понижать температуру, то в момент появления жидкости один из концов должен сделаться тяжелее, и при нагибании трубки жидкость опять начнет переливаться. Таким образом явится возможность определить как момент полного испарения, так и конденсации” [11, с. 163].
Свой прибор, основанный на этой идее, Надеждин назвал "дифференциальным денсиметром” (рисунок). Работая в течение многих месяцев над его усовершенствованием, он создал конструкцию, вызвавшую восхищение современника: ”Прием, предложенный им, до такой степени прост и оригинален, что, по всей вероятности, им скоро станут пользоваться и другие экспериментаторы” [81, с. 242].
Этого, однако, не произошло. Хотя описание прибора Надеждина вошло в солиднейшие руководства по физике и физической химии (В. Оствальда [82], О.Д. Хвольсона [83], К. Йеллинека [84]), но никто, кроме автора, такого прибора не воспроизвел и не применил. Очевидно, несмотря на простоту принципа, реализация его требовала очень большого искусства.
Надеждин измерил этим способом критические температуры двуокиси азота, брома и воды [8, 9]. Первое в науке выполненное Надеждиным в 1885 г. прямое (13) экспериментальное определение критической точки воды Столетов назвал "кульминационным пунктом деятельности Киевской лаборатории” [27, с. 422].
Надеждин не считал полученный для воды результат (358°С) окончательным; позже он писал: ”К сожалению, поразительно малая величина критического объема заставляет смотреть на полученную нами величину критической температуры лишь как на первое приближение” [11, с. 155].
a b
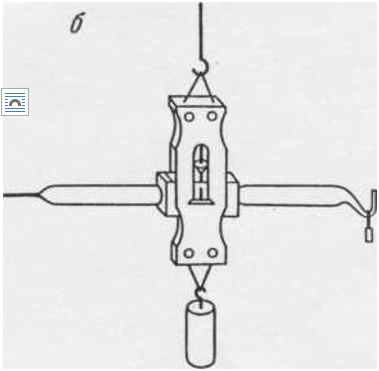
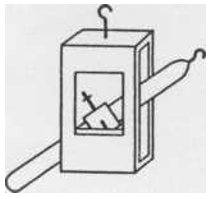
Дифференциальный денсиметр А.И. Надеждина
а — первоначальный (1884), б — окончательный вариант (1885)
Возможно, что заниженное против ныне принятого (374°С) значение критической температуры воды получилось у Надеждина из-за присутствия растворенного воздуха.
В течение немногих лет он измерил критические температуры для 35, критические давления — для 23 и критические объемы — для 20 веществ. К 1887 г. в мировой литературе было опубликовано всего 164 определения критических температур, 89 определений критических давлений и 32 критических объемов (см. сводку в [85]).
Это значит, что Надеждин один получил свыше четверти всего фонда данных по критическим параметрам, который был собран в науке к концу его жизни!
Большинство определений Надеждина в настоящее время пересмотрено: за истекшее столетие повысилась и точность измерений, прежде всего поддержания постоянства условий, и, главное, чистота веществ. И все же мощь сделанного им такова, что доныне некоторые из его цифр сохраняются в справочниках! В последних изданиях и международных таблиц Ландольт- Бернштейна [86] и отечественного "Справочника химика” [87] помещены найденные Надеждиным критические данные для 1,1 и 1,2-дихлор¬этана, для изобутилового спирта, для этиловых эфиров масляной и изомасляной кислот и метилового эфира валерьяновой кислоты. Какой экспериментатор не мечтал бы о таком долголетии своих цифр!
Теоретическую сторону дела Надеждин не разрабатывал и природу критического состояния не обсуждал: до разгара дискуссий на эту тему он не дожил. Но ему, очевидно, пришлось пройти через туман неясностей, в котором первоначально блуждал и его учитель. Так, в первой своей статье Авенариус утверждал: «Температура полного испарения жидкости в герметически замкнутом объеме не зависит от этого объема, а следовательно, и от давления, которому подвергается жидкость» [77, с. 309]. Вскоре Авенариус выдвинул и другой неверный тезис — о том, что при критической температуре удельные объемы жидкости и пара могут не совпадать [88].
Эти положения были приняты за истину и в основной статье Зайончевского 1878 г. [36]. После выхода в свет немецкого издания ”Непрерывности” Ван-дер-Ваальса [89] и критики Столетова [90] Авенариус принял взгляд Эндрюса и Ван-дер-Ваальса и изложил его в статье 1884 г. [91]. Все это было пережито Надеждиным, когда он писал: "Можно считать доказанным, что критическое состояние обусловливается равенством удельных объемов пара и жидкости” [11, с. 69] ("Необходимость такого равенства стала очевидна лишь после работ Andrews’a, van der Waals’а и других” [11, с. 162]), и, пренебрегая пиететом, отмечал: ”придя в своей работе к ошибочному заключению, что объемы пара и жидкости не равны при критической температуре, г. Авенариус допускал существование 3-й промежуточной кривой [объем-температура. — А.К. ], которой и соединяются кривые пара и жидкости” [Там же, с. 105].
Создание дифференциального денсиметра и основывалось как раз на хорошем понимании теоретического положения об уравнивании плотности жидкости и пара в критической точке.
Прозрачные утверждения классической теории критического состояния начали ревизоваться вскоре после смерти Надеждина. Причин этому было несколько: присутствие газовых примесей (воздуха и др.), меняющих поведение системы в критической области; разложение вещества при нагревании; неизотермичность содержимого в рабочем объеме прибора (точность поддержания температуры обычно не достигала даже 0,1—0,2°, которых добился Надеждин); медленность установления равновесия в отсутствие перемешивания. Если самому Надеждину удалось избежать ошибок, то в дальнейшем обилие неточных и неточно интерпретируемых наблюдений породило подлинную путаницу и хаос в теоретическом описании критического состояния (в России инициатором пересмотра был Б.Б. Голицын). В защиту классической теории выступил А.Г. Столетов, подробно разобравший "ереси” "неверующих и мудрствующих” [92] в статьях о критическом состоянии тел [74, 90, 93], и несколько позже И.П. Кюнен, впервые применив¬ший в своих измерениях электромагнитное перемешивание. Достойно внимания, что именно работы Надеждина дали фактическую основу замечательным критическим разборам Столетова. Споры, однако, не улеглись, а после смерти Столетова возобновились с еще большей страстью. Период разброда и шатаний в учении о критических явлениях завершился уже в конце 1900-х годов возвратом на классические позиции — но на гораздо более высоком экспериментальном уровне, чем во времена Надеждина. (Множество подробностей, относящихся к западноевропейским исследованиям, содержится в работе [94]).
7. ДАВЛЕНИЕ НАСЫЩЕННОГО ПАРА
С исследованием критических явлений тесно связаны измерения Надеждиным давления насыщенного пара жидкостей при высоких температурах. Пользуясь методикой Зайончевского, Надеждин получил данные для 12 сложных эфиров жирного ряда в интервале от точки кипения до критической. "Одни его определения упругости паров в этой работе стоят, по моему мнению, докторства”, — писал Авенариус Столетову при посылке "Этюдов” [32].
Эти экспериментальные данные тоже частично сохранили значение до нашего времени [86, 87]. Для описания своих данных Надеждин вслед за Зайончевским и Ван-дер-Ваальсом использовал трехпараметричекую формулу Роша
р = аb t/(m+t) (1)
где р — давление насыщенного пара при температуре t; а, b, m— параметры. В наше время было показано [95, с. 113], что из трехпараметрических формул для целей экстраполяции и сравнительного расчета наилучшим является близкое к (1) по форме уравнение Антуана, предложенное уже после смерти Надеждина:
lg p = a – b/(m + t)
Однако интересен не сам по себе этот выбор, а наглядная демонстрация связи между различными алгебраическими формулами, предложенными для температурной зависимости давления насыщенного пара. Смотря по тому, какой функцией от температуры представлено отношение теплоты испарения L к изменению объема при испарении uв уравнении Клапейрона—Клаузиуса, интегрированием последнего можно получить любую из предложенных формул [11, с. 136—138]. По-видимому, в термодинамической литературе до Надеждина такой демонстрации проведено не было. Это один из редких в то время примеров сочетания собственно уравнений термодинамики с моделью, в рассматриваемом случае непосредственно с математической моделью (алгебраической формулой) для получения искомой зависимости в виде алгебраического уравнения.
С идеей модели в термодинамике мы встретимся еще раз при обсуждении термодинамического подобия.
8. ТЕРМОДИНАМИЧЕСКОЕ ПОДОБИЕ
Термин "термодинамическое подобие” появился в науке лишь в середине нашего века. (Впервые в 1952 г. одновременно в книгах [96, 97]. Подробное обсужден понятия (с несколько различающихся позиций) см. в книгах [98-102]). Однако уже Гиббс намеревался исследовать ”подобие в термодинамике” [103, с. 418], а Камерлинг-Оннес [63] впервые указал на связь закона соответственных состояний с идеей подобия в механике (подобными Оннес считал молекулы, различающиеся только масштабом размеров и межмолекулярных сил). Предыстория же учения о термодинамическом подобии началась задолго до Надеждина.
С высоты нашего времени явственно усматриваются две основных линии в физике и химии, породившие это учение. Одна состояла в приложениях сравнительного метода21 к изучению веществ. (По-видимому, первый ряд сравнения в естествознании представляет таблица сродства Э. Жоффруа (1718)). С этой линией связаны многие крупные имена (Дж. Дальтон, А. Авогадро, Ж. Л. Люссак), но оформление ее в особое научное направление принадлежит Г. Коппу. Преданный идее связи химического состава и физических свойств веществ, Копп провозгласил использование рядов сравнения для нахождения неизвестных свойств (1842); в рамках правил аддитивности он пытался развить "стехиометрию физических свойств химических соединений” (1855). В сочинении II. Де Гена [104] эта область исследований получила и характерное название "сравнительная физика”. Другая линия, ответвившаяся от первой и также многим обязанная Коппу (1842-1844), характеризовалась поисками специальных, "соответственных” (Дальтон) условий для сравнения. Установление понятия о критическом состоянии дало этим поискам новый импульс. ”Мне кажется, — писал Менделеев в 1870 г., — что изучение температуры абсолютного кипения покажет очень характерные отношения с составом тел. Если Копп двинул вопрос вперед, сравнивая объемы тел при температурах их кипения, то несомненно, что сравнение их объемов при температурах, когда их сцепление становится почти нулевым, будет представлять еще более интереса...” [105, с. 110]. Десятилетием позже Ван-дер-Ваальс оправдал справедливость этих слов.
Работы Надеждина приходятся на время, когда каждое из упомянутых направлений достигло некоторого логического конца. Поиски "соответственных” условий увенчались открытием "принципа соответственных состояний” (это не значит, что Ван-дер-Ваальс ставил себе именно такую задачу (см. [71, с. 116, 241]); логика развития научного направления и логика отдельного научного открытия совпадают редко). Что же касается "сравнительной физики”, то здесь сделалось ясным, что ”к каким-нибудь выводам”, по словам Надеждина, можно прийти, только выбирая ”из бесчисленного множества соединений... ряды или группы с аналогичными свойствами: гомологи, изомеры, производные одних и тех же радикалов” [2, с. 536].
В конце концов, суть каждого из направлений сводится к простым положениям: сравнивать вещества при подобных условиях, сравнивать подобные вещества. Оставалось соединить эти программы: необходимо сравнивать подобные вещества в подобных условиях. Надеждин оказался одним из первых ученых, с чьих трудов и начинается объединение обеих программ в будущее учение о термодинамическом подобии.
Уже первое его исследование, пока безотносительно к намерениям автора, оказывается на стыке обеих программ. Определяя критическую температуру различных фракций, отогнанных из продававшегося амилена, он нашел, что ”на сколько возвышалась температура кипения, на столько же повышалась и температура абсолютного кипения” [1, с. 160]. Вскоре эта зависимость была проверена на индивидуальных углеводородах [2] и подтвердилась для гомологов и изомеров. "Для всех подобных (14) тел, — заключает Надеждин, — получен интересный вывод: критическая температура, являясь, подобно температуре кипения, некоторым пунктом (хотя бы и предельным) совместного существования пара и жидкости, будет выражаться функцией того же вида от частичного веса и строения, как и температура кипения” [2, с. 541]. Развивая эту тему дальше, Надеждин заключает, что разность критических температур tкр двух близких тел (изомеров или гомологов) должна быть равна разности нормальных температур кипения. Это означает переход от общих соображений относительно подобия свойств веществ непосредственно к сравнительному расчету, т.е. „к возможности очень просто и точно вычислять критические температуры очень многих рядов органических соединений, а в некоторых случаях по критическим температурам — температуры кипения” [Там же]. Например, для олефинов нормальная точка кипения
tн.т.к.= tкр– 156,6.
Найденная Надеждиным закономерность многократно обсуждалась в литературе [106—108], в том числе и самим автором — в ”Этюдах” [11, с. 78—86]; ее иногда называют правилом Надеждина-Павлевского.
"Этюды”, "замечательная по своей содержательности монография Надеждина” [100, с. 265], уже перерастают границы традиции. Сначала кажется, что в исходной постановке вопроса автор следует Де Гену — от названия до утверждения, что высшим достижением сравнительного метода в науке является периодический закон Менделеева (15) [11, с. 4]. В дальнейшем, однако, становится все более явной оригинальность труда Надеждина, и особенно в рассматриваемом отношении.
Если Де Гену "остается, по-видимому, совершенно неизвестной” [Там же, с. 7] теория Ван-дер-Ваальса, если, с другой стороны, сам Ван-дер-Ваальс в поисках универсальности отвлекается от групп аналогичных веществ, то Надеждин оказывается первым на этом "перекрестке идей”, именно с его работ начинается объединение названных ранее направлений.
Так, рассмотренные только что правило и найденная Де Геном закономерность для коэффициентов расширения (α) гомологов
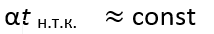 (2)
(2)
связываются через принцип соответственных состояний. Из последнего Надеждин выводит, что
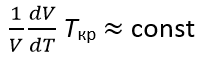 (3)
(3)
Так как множитель при Ткр, есть α, то, заключает автор, ”для таких рядов Tкр—tн.т.к.= const” [Там же, с. 80].
Это заключение не очевидно. Однако Надеждин слишком увлечен собственным правилом и этого не замечает. Гораздо естественнее был бы вывод, сделанный позже К.М. Гульдбергом [111], о постоянстве отношения tн.т.к.и Т кр, а не их разности.
Проверяя на 35 веществах, "насколько закон соответствующих объемов будет общим законом” [11, с. 99], Надеждин находит, что при температурах до точки кипения безразмерное отношение (3) постоянно в пределах 3%, лишь для метилового и этилового спиртов и для хлороформа отклонения достигают 7%.
До Надеждина столь обстоятельному испытанию принцип соответственных состояний не подвергался — хотя бы уже только из-за отсутствия необходимых данных. Еще более подробно исследует Надеждин применимость принципа соответственных состояний Ван-дер-Ваальса к давлениям насыщенного пара и находит, "что это закон действительно общий” [Там же, с. 145].
Представление р—V—T-зависимостей в приведенных переменных исключает индивидуальные характеристики веществ. Понимая это, Надеждин, как и все его современники, не может освободиться от потребности связать эти зависимости с формой первоначального уравнения состояния — Ван- дер-Ваальса или Клаузиуса. И поэтому эмпирическую зависимость
π = f (τ) (π и τ – приведенные давление и температура на линии насыщения)
сравнивает с ''теоретическими ”, выведенными из этих уравнений состояния; сравнение говорит в пользу уравнения Клаузиуса.
В ходе исследования систематически вычисляются параметр f в предложенной Ван-дер-Ваальсом в 1881 г. [89, с. 147] формуле (16)
-lnπ= f(1- τ)/τ
и величина (dπ/dτ)кр, которая в соответствии с этой формулой должна быть равна f/lge. Для изученных Надеждиным веществ последняя величина близка к 7, согласуется с уравнением Клаузиуса. Но наиболее интересно следующее утверждение: "Строго говоря, каждое вещество имеет свой собственный ход π = f (τ); полное совпадение получается лишь для веществ, близких по своим свойствам” [11, с. 154]. Здесь с очевидностью выступает соединение принципа Ван-дер-Ваальса с условием сравнения подобных веществ. Предложение К.А. Путилова назвать безразмерный параметр f "критерием Ван-дер-Ваальса-Надеждина” [100, с. 284] — вполне оправданный способ напомнить о вкладе талантливого физика в подготовку теории термодинамического подобия.
Последующими работами [112-114] принцип соответственных состояний был освобожден от связей с конкретными формами уравнения состояния; были установлены также, в особенности в многолетних исследованиях С. Юнга (1892—1910), закономерности отклонений этого принципа для различных групп веществ [115, 116]. Необходимость разработки принципа соответственных состояний на основе общей теории подобия осознавалась и провозглашалась по мере развития этой последней; поэтому существенные сдвиги приходятся уже на середину нашего столетия [96— 102]. Один из главных результатов: для "нормальных” (неассоциированных) флюидов безразмерное (приведенное) уравнение состояния включает лишь один безразмерный параметр (определяющий критерий подобия) (подробнее см. [101]).
Для ассоциированных веществ предложены дополнительные параметры, характеризующие "степень сложности межмолекулярного взаимодействия”, или "степень полярности” молекул.
9. МОДЕЛИ В ТЕРМОДИНАМИКЕ И СТРОЕНИЕ ЖИДКОСТЕЙ
Термодинамическое подобие имеет и еще один аспект, связанный с проблемой "модели в термодинамике”. Эта проблема также обязана Надеждину интересными подходами, она может быть сформулирована следующим образом. Информация, необходимая для «оплодотворения термодинамики» [117,с. 7],воплощается либо непосредственно в виде конкретных экспериментальных данных, либо в виде модели одного из трех классов: физической (система, подобная изучаемой в рассматриваемом отношении; именно такие модели — предмет теории термодинамического подобия); структурной (представления о строении объекта, из которых затем выводятся соотношения, дополняющие уравнения термодинамики(17); аналитической (непосредственно те или иные формулы, например уравнения состояния).
Надеждин почти не занимался термодинамикой как таковой, но необходимость в тех или иных моделях (в указанном смысле) для приложений термодинамики он осознал раньше, чем большинство его современников. В докладе 1884 г. [16] он говорил о двух путях в развитии "механической теории теплоты”. Первый заканчивается общими уравнениями — это ”путь аналистов”, второй же — ”путь научного синтеза” — уходит дальше: ”делая aprioriпредположения относительно значения количеств, входящих в алгебраической форме в общие уравнения, аналитически искать между ними соотношения и проверять на опыте полученные результаты” [16,с. II].
Один из примеров того, как двигался Надеждин по этому пути, был приведен в разделе 7; обсуждение связи между формулами для давления насыщенного пара основано на введении аналитической модели в уравнение Клапейрона-Клаузиуса.
Другой пример дает работа Надеждина ”0 теплоемкости жидкостей” [6, 7]. Здесь "преимущества” сочетания уравнений термодинамики с "основными предположениями о свойствах той среды, в которой происходят тепловые явления”, Надеждин видит в возможности выбора определенной модели жидкого состояния. Для конденсированных веществ можно допустить либо ”то же частичное строение, что и в газах”, как это делают Ван-дер-Ваальс и Клаузиус, либо принять "прямо противоположное” представление, "именно что, подобно тому как частицы образуются из атомов, должно являться соединение частиц в более сложные группы, различные для различных агрегатных состояний, и что такие сложные группы и составляют в твердых и жидких телах физические частицы, к которым мы и должны относить различные теоретические соображения ... последняя теория строения, поддерживаемая Пикте, Де Гееном, Л. Мейером и мног[ими] друг [ими], является не менее, если не более вероятной, чем первая” [6, с. 234].
Представление о различной степени сложности частиц газа и жидкости, шедшее еще из домолекулярной эпохи, пошатнулось, но все же сохранилось в науке после появления знаменитой теории Ван-дер-Ваальса, основанной на постулате об идентичности молекул газа и жидкости (18). Надеждин, который многократно и с глубочайшим уважением цитировал труд Ван-дер-Ваальса – „этот самый блестящий образец научного синтеза прошлого десятилетия” [11, с. 7], тем не менее явно принял противоположную т зрения (см. также [11, с. 31]).По-видимому, его привлекла выработанная им простая схема: "Отношение количества тепла, идущего на обращение в пар какого-нибудь количества жидкости, к количеству тепла, необходимого для нагревания на 1°, будет пропорционально числу химических (газообразных) частиц в одной физической (жидкого тела)“ [6, с. 236].(Заметим, что здесь атомизм из лозунга превращается в инструмент для построения последовательной концепции жидкого состояния.) Исходя из этой идеи Надеждин заключил, что если взять две жидкости при таких температурах, что их удельные объемы составят равные доли критических объемов, то ”при соответственных плотностях отношение теплоемкостей равняется отношению теплот испарения, умноженному на обратное отношение критических давлений” [15, с. ХСIХ], поскольку, по его мнению, критическое давление должно быть пропорционально "числу химических частиц, соединяющихся в одну частицу жидкого тела“. Это дает формулу
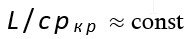
хорошо согласующуюся с опытными данными для умеренных (близ 0°C) температур, в особенности для групп близких веществ. (Здесь L— теплота испарения, с —теплоемкость, ркр —критическое давление.)
Это исследование Надеждин продолжить не успел. Но замысел использования сравнительного метода для суждения о строении (степени ассоциации) тех или иных жидкостей сохраняет интерес. И он же подводит к выводу об эффективности комбинирования структурных и физических моделей в термодинамике; оно действительно используется в современных работах по термодинамическому подобию.
Что же касается строения жидкостей, то сейчас позиция Надежда представляется наивно-прямолинейной, но ее рациональное начало сохраняет свое значение (19).
10. МОТИВЫ НАУЧНОГО ТВОРЧЕСТВА
Вместо заключения хотелось бы привести несколько отрывков из речи [4],в которых отразилось отношение Надеждина к науке, — оно приводит на память знаменитое выступление Эйнштейна "Мотивы научного творчества”.
"Никогда естественные науки: в особенности химия и физика, образующие теоретическую основу всех других ветвей естествознания, не имели такого широкого и плодотворного применения, как в наше время. Уже одного значительного влияния естественных наук на строй промышленной, общественной и политической жизни народов было бы достаточно, чтобы безучастно не мог пройти ни один деятельный член общества, не вопрос имеет и другую сторону” [4, с. 3].
"Общество начало интересоваться не только теми или другими применениями науки о природе, которые сами по себе не составляют науки, хотя часто и принимаются за таковую, но и самим могущественным методом как источником знаний и воспитательным средством, и теми выводами, окончательными или временными, к которым приходили ученые в той или другой области наук” [4, с. 5].
"...Всякое обобщение, всякое упрощение, которые мы вносим своим открытием в беспредельную сменяемость и разнообразие явлений, имеет несравненно более значения, чем кажущаяся оригинальность открытия или вытекающие из него практические приложения.
В обществе же обыкновенно, наоборот, в особенности часто встречаемся с оценкой научных трудов масштабом практического применения” [4, с. 29].
"Требовать от естественно-научных открытий непременно и прежде всего практичности, конечно, более справедливо, чем искать осязательных результатов пользы языкознания, истории и т.п., но и тут такое требование является неосновательным, так как оно опровергается всем историческим ходом науки” [4, с. 30].
"Дело в том, что наука сама по себе духовное благо и в себе самой находит для себя удовлетворение” [4, с. 31].
”Что же касается до двигательной силы в науке, то побуждением всех исследователей является вечное неугасимое стремление, составляющее бесспорно самую высокую черту человеческой деятельности, — стремление познать истину, поднять хоть край закутывающего ее покрывала, хотя бы за это познание, как в прекрасной легенде о Саисском храме, нужно было заплатить смертью или, по крайней мере, годами тяжелой, часто неведомой миру борьбы и неведомых ему лишений. Для своих последователей наука делается высоким долгом и вместе настоящею страстью, но страстью самой бескорыстной, самой чистой, самой светлой из всех страстей человечества” [Там же].
Этими словами лучше всего и закончить рассказ об Александре Ивановиче Надеждине.
1. Предметы были такие: общая физика (5), общая химия (3), начертательная геометрия (4), тригонометрия (5), алгебраический анализ (4), дифференциальное исчисление и интегрирование функций (5), аналитическая геометрия (4), сферическая астрономия (5), теория чисел (4), богословие (4).
2. Владимир Иванович Зайончевский (1842?—1908) [34, 35],сын обер-офицера, в 1860 г. окончил с золотой медалью Немировскую гимназию и поступил на физико- математический факультет Киевского университета, который закончил в 1864 г. по математическому отделению. В том же году занял должность консерватора физического кабинета, а с 1874 г. совмещал ее с работой "лаборанта физической лаборатории”; в 1870-1878 гг. одновременно работал преподавателем в Киевской женской гимназии; в 1865 г. выдержал испытания на степень кандидата математических наук. С 1878 по 1888 г. преподавал физику и метеорологию в Ново-Александрийском институте сельского и лесного хозяйства. Главная работа — "Определение упругости паров некоторых жидкостей при высоких температурах” [36] (см.также [37]).
3. Кассиан Николаевич Жук (1844-1917) [38], сын военного врача, окончил 2-ю Киевскую гимназию и затем, в 1870 г. физико-математический факультет Киевского университета. Работал преподавателем в средних учебных заведениях Киева, а в 1878г. заменил Зайончевского в должности хранителя физического кабинета и оставался в ней до конца 1890 г. С 1899г. и до конца жизни - преподаватель сельскохозяйственной метеорологии и наблюдатель метеорологической обсерватории Киевского политехникума. В лаборатории Авенариуса выполнил важные исследования по расширению жидкостей при высоких температурах [39, 40],затем занимался метеорологией и климатологией.
4. Оскар Эмильевич Страус (1856—?),сын киевского врача, в 1880г. окончил Санкт-Петербургский университет со степенью кандидата; летом 1880г. в лаборатории Авенариуса выполнил главную экспериментальную работу [41];вернувшись в Петербург, дополнил свои измерения и опубликовал интересную теоретическую обработку своих данных [42].В дальнейшем занимался организационной и издательской работой в области электротехники; с 1896г. вновь жил в Киеве, возглавляя электротехнический отдел редакции журнала "Инженер” вплоть по прекращения этого издания в конце 1917 г.
5. Для иллюстрации - цитата из воспоминаний Д.А. Гольдгаммера о столетовских лекциях 1881 г. в Московском университете: ”. . . совсем новые в то время исследования о критической температуре и изложение только что переведенной на немецкий язык знаменитой статьи vanderWaals’a— все вводило слушателей в область самых жгучих, самых интересных вопросов времени и вызывало захватывающий интерес” [46, с. 46].
6. Впоследствии занятия философией отразились в выступлении Надеждина [4], во введении к которому обозначены «две загадочные области: область духа с его деятельностью и область природы, к которой принадлежит и сам человек своей материальной стороной» и подчеркнута необходимость «опытного исследования в естествознании, необходимость, которую признали лишь в настоящем столетии»
7. Теоретическая астрономия, практическая астрономия, разностное исчисление, теория вероятностей, статика, динамика, вариационное исчисление, интегрирование дифференциальных уравнений, приложение дифференциального и интегрального исчисления к геометрии, определенные интегралы, эллиптические функции, небесная механика, геодезия, теоретическая физика, метеорология.
8. Новый министр просвещения И.Д. Делянов поставил задачей "привести наши университеты из рассадников политической агитации в рассадники науки”. В новом уставе "подчинение университетов сильной правительственной власти выразилось прежде всего в расширении средств надзора со стороны Министра” [55, с. 613, 616].
9. И сразу же Надеждин должен был подписать обязательство: ”в случае выдержания мною в течение трех лет испытания на степень магистра выслужить в высших учебных заведениях двухлетний срок за каждый год получения стипендии” [Там же, л. 12]. На случай провала на этих испытаниях предусматривались либо возврат сполна полученной стипендии, либо служба в средних учебных заведениях.
10. Уместно подчеркнуть, что учение о теплоте оставалось последней областью, не преобразованной законом сохранения энергии, поскольку он не был согласован с принципом Карно. Только после того как в 1850 г. оба принципа удалось совместить и таким образом построить "механическую теорию теплоты”, торжество закона сохранения энергии стало полным.
11. Н. Деллингсхаузен (1827-1896), выпускник Дерптского университета, эстонский помещик, в своем "кинетическом учении о природе” [67,68] исходил из того, что ”нет наблюдений, доказывающих существование границы делимости материи” [68, с. 9], и пытался объяснить все физические и химические явления изменениями движения общего всем телам неизменного субстрата „не прибегая к предположениям об атомах, о молекулярных силах и о невесомых” [69, с. 1].
Л.Б.Сталло (1823-1890) учился в США первоначально физике и математике, а затем юриспруденции и работал преимущественно адвокатом. Свое главное сочинение "Понятия и теории современной физики” впервые опубликовал в 1881 г.; оно выдержало по нескольку изданий в Англии, США, Германии и Франции. Последний раз эта интеллектуальная и прекрасно написанная книга вышла под редакцией П.У. Бриджмена в 1960 г. [70].
12. Не лишне привести одну цитату из книги Сталло: "Может показаться странным, что столь многие лидеры научного исследования, прошедшие серьезную школу точного мышления и строгого анализа, тратили усилия на теорию, так явно противоречащую всякой научной трезвости, — на гипотезу, в которой как раз то самое, что подлежит объяснению, есть лишь малая часть предположений, принимаемых для объяснения <...> Иллюзия, что упругость твердого атома меньше нуждается в объяснении, чем упругость большого газового тела, тесно связана с фантазией, что бездна между миром материи и разумом может быть сужена, если не перекрыта мостом посредством разрежения материи или разрешения ее в силы” [70, с. 151].
13. Косвенное определение - по критическим температурам водно-спиртовых смесей незадолго до того, в 1881 г., было осуществлено Страусом [42]
14. Это еще не термин. В другом месте - "близкие” тела.
15. Вполне естественно, что Надеждин послал Менделееву экземпляр "Этюдов” ”в знак глубочайшего уважения от автора” [109]. Менделеев же причислил книгу Надеждина к важнейшим сочинениям своей громадной библиотеки [110].
16. Надеждин продемонстрировал также связь этой формулы с формулой Роша [11, с. 156].
17. Строгий путь статистической механики - построение статистических сумм на основе структурной модели - для большинства реальных систем непроходим, и на том или ином расстоянии от идеала, т.е. от вывода из первых принципов, вводятся допущения о значениях параметров или формах функций, входящих в уравнения статистической механики.
18. Прекрасное рассмотрение противостояния этих двух концепций, но только в исследованиях критических явлений дала И.М.Х. Левельт-Сенгерс [94].
19. Более чем вековая история представления об образовании ассоциатов в жидком состоянии не закончена и ныне; это представление следует рассматривать в контексте возникновения, становления и развития более общего понятия "кластер”, весьма популярного в современной науке.
ПРИЛОЖЕНИЕ1 [50]
А .И. НАДЕЖДИН
ЭКСПЕРИМЕНТАЛЬНОЕ И ТЕОРЕТИЧЕСКОЕ ИССЛЕДОВАНИЕ ИЗМЕНЕНИЯ АГРЕГАТНОГО СОСТОЯНИЯ ТЕЛ
Большая часть известных нам тел может находиться — в зависимости от своего теплового содержания — в трех видах: твердом, жидком и газо- или парообразном. Уже с давних пор были замечены опытные законы, наблюдавшиеся при переходе тел из одного такого состояния в другое: 1) постоянство температуры [здесь и далее выделено А. И. Надеждиным. В квадратных скобках вставлены необходимые пояснения или уточнения. - А.К.]и находящееся в тесной связи с этим поглощениеили выделение тепла(впервые замечено DeLuc’ом в XVII в. [по современному исчислению – в XVIIIв.]); 2) влияние давления на кипениеи, наконец, изменение объема.
До появления механической теории тепла, т.е. до 50-х годов нашего века, исследование изменений агрегатных состояний было по необходимости эмпирического характера; изучались главным образом особенности этих изменений и их зависимости от посторонних условий: сосудов, растворенного воздуха, вида свободной поверхности и т.п. Механическая же теория тепла в непродолжительном времени по своем возникновении не только выяснила теоретическую необходимость большинства выведенных особенностей, но открыла между ними связь и могла вывести новые.
Но надо признаться, что полной теории изменения частичного строения, теории, обнимавшей бы собою все наблюдающиеся законы и особенности, мы не имеем: во-первых, по недостатку точных опорных данных относительно большинства тел, во-вторых, по неимению законченной теории тел вообще.
Всякое состояние может быть определено тремя величинами из пяти, характеризующих вообще различные состояния тел: удельного объема V, давления р,температуры τ (считаемой от абсолютного нуля), энергии ε и энтропии η).
Зависимость между тремя из них, определяющая термодинамические свойства тела, f(х, у, z), называется уравнением состояния тела (с аналитической точки зрения) и термодинамической поверхностью (с геометрической). Если бы нам была известна такая зависимость, то мы имели [бы] полную теорию как изменений вообще, так и изменений агрегатного состояния. Но, как известно, существуют только попытки к нахождению такой функции, именно: VanderWaals‘а и Clausius’а для жидких игазообразных состоянийиGibbs’а и Planck’а для всех трех [состояний]. Почему под исследованием изменений частичного строения подразумевают лишь приложение к ним основных формул механической теории тепла.
Возьмем переход из твердого состояния в жидкое, так называемое плавлениеи обратный — замерзание.По уравнению Clausius’а, выведенному на основании второго начала М.Т.Т. [механической теории теплоты], количество приведенного к телу тепла может быть представлено
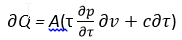
где с— теплоемкость, А —термический эквивалент.
Опыт показ[ывает], что температура плавления постоянна, след[овательно],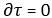 и
и
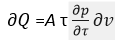 В момент плавления тело состоит из твердого тела и жидкости. Обозначая через ω удельный объем жидкости, Ω — твердого тела и μвес жидкости, получим
В момент плавления тело состоит из твердого тела и жидкости. Обозначая через ω удельный объем жидкости, Ω — твердого тела и μвес жидкости, получим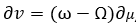 и, след[овательно] ,
и, след[овательно] ,
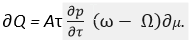
Так выражается тепло, необходимое для расплавления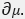 , для расплавления единицы веса, или
, для расплавления единицы веса, или
скрытое тепло =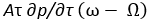 (1)
(1)
Обозначим его α. Целый ряд наблюдений, начиная с Black’а, Wilke[Wilcke] и Craffod’а [Crawford] в XVII в. и кончая Hess’ом, Person’ом и Bunsen’ом, показали, что это скрытое тепло, или теплота плавления, положительна.Из уравнения (1), выведенного в 1850 г. Джемсом Томсоном, мы видим, что температура плавления должна зависеть от давления, что и не подозревали прежние исследователи. Зависимость эта определяется
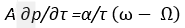
Знак производной зависит от знака 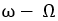 Следовательно, для некоторых тел температура плавления повышается, для других наоборот. Действительно, Bunsenпоказал, что для спермацета, для которого ω > Ω, при увеличении давления на 150 атм температура плавления повышается на 12o. Отсюда интересен вывод в области геологии, что, несмотря на высокую температуру, большая часть земного ядра может находиться в твердом виде. Но существуют тела, для которых ω < Ω, напр[имер] вода, сурьма и др. Если примем для воды число Реньо и Персона α = 79,25 са1, то
Следовательно, для некоторых тел температура плавления повышается, для других наоборот. Действительно, Bunsenпоказал, что для спермацета, для которого ω > Ω, при увеличении давления на 150 атм температура плавления повышается на 12o. Отсюда интересен вывод в области геологии, что, несмотря на высокую температуру, большая часть земного ядра может находиться в твердом виде. Но существуют тела, для которых ω < Ω, напр[имер] вода, сурьма и др. Если примем для воды число Реньо и Персона α = 79,25 са1, то 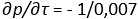 , т.е. с увеличением давления на 1 атм точка плавления понижается на —0,007°. Знаменитый брат Дж. Томсона, сэр В. Томсон, проверил этот вывод на опыте и нашел понижение -0,0078°.
, т.е. с увеличением давления на 1 атм точка плавления понижается на —0,007°. Знаменитый брат Дж. Томсона, сэр В. Томсон, проверил этот вывод на опыте и нашел понижение -0,0078°.
Позднее Муссону удалось понижать температуру плавления до —18° и даже —20°, а Бунзен и Гопкинс показали то же для других тел. Отсюда объясняют явления перезамерзания (regelation), пластичности льда и причины движения глетчеров. Обратное явление — замерзание — менее правильно [менее регулярно]. Каждое тело может быть охлаждено до температуры значительно ниже той (до 20° ), при которой происходит отвердевание, что замечено еще Фаренгейтом и подтверждено многочисленными исследования [ми] Депреца и Жернеса. Механическая теория тепла показывает, что в этих случаях скрытое тепло (выделяемое) будет меньше, чем при нормальных условиях. Обозн[ачим] скрытую теплоту в первом случае α', во втором α, пусть c— теплоемк[ость] твердого тела, c' — жидкого. Мы можем 1 [единицу] веса перевести от темпер[атуры] τ (плавления) к τ — θ [θ— величина переохлаждения в градусах] двояким путем: или заставив его отвердеть и охладиться, 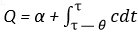 или же переохладиться
или же переохладиться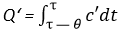 Но так как внутренняя энергия и внешняя работа та же, Q= Q‘ и
Но так как внутренняя энергия и внешняя работа та же, Q= Q‘ и
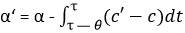 (2)
(2)
Опыт показывает, что теплоемкость жидкости больше теплоемкости твердого тела, след[овательно], α> α‘.Что же касается до изменений объема при плавлении, то для объяснения этого явления нужны уже вспомогательные гипотезы.
Испарение.Так как законы, замечаемые при переходе из твердого состояния в жидкое и из жидкого в парообразное, схожи, то и зависимость между v, ри τ будет того же вида. Идя тем же путем, как при выводе (1), получим для скрытого тепла испарения или просто теплоты испарения r выражение
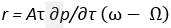 (3)
(3)
где ω — уд[ельный] объем пара. Ур[авнение] (3) выведено еще Клапейроном в форме
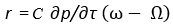 где С— функция от температуры, которую он называл функцией Карно. В первом же своем мемуаре 1850 г. Клаузиус показал, что С=А (t+ 273).
где С— функция от температуры, которую он называл функцией Карно. В первом же своем мемуаре 1850 г. Клаузиус показал, что С=А (t+ 273).
Здесь мы аналогично с плавлением можем вывести, что если жидкость приходит в кипение при определенном давлении, то maximumскрытого тепла будет соответствовать кипению при нормальных условиях, так как если жидкость не имеет свободной поверхности, то мы можем перегреть ее до некоторой температуры ![]() ,если τ — температура кипения при нормальных условиях. Поступая., как при выводе (2), получим
,если τ — температура кипения при нормальных условиях. Поступая., как при выводе (2), получим
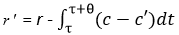
Так как с[теплоемкость жидкости] больше c‘ (теплоемкости пара), r> r‘.
Исследуя зависимость испарения от давления, мы получаем
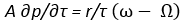
всегда положительно; удельный объем пара ω всегда больше [чем удельный объем жидкости], следовательно ω-Ω также положительно, а следовательно, и др/дτ также положительно,т.е. точка кипения для всех тел повышается с давлением.Спрашивается, до каких пор может идти это возвышение?
Если возьмем жидкость в запаянной трубке, то, очевидно, температура может возвышаться, лишь пока ω не сделается равным Ω и исчезнет, следовательно, различие между жидкостью и паром. Такое состояние, называемое теперь критическим,будет, следовательно, характеризоваться условием ω = Ω и r= 0. Действительно, опыты Реньо, произведенные для проверки законов Уатта и Соутерна, показали, что rможет быть выражено функцией такого вида:
а - bt- ct2,следовательно, стремится к 0. Но так как определение r не производится при строго постоянном объеме, то более удобно брать для определения критического состояния выражение для внутренней скрытой теплоты ρ = r– Ap(ω-Ω).
Вычисление и опытная проверка были произведены проф. Авенариусом, и совпадение оказалось весьма удовлетворительным. Не ограничиваясь этим, мех. т.т. позволяет исследовать даже и такие, долгое время одиноко стоящие явления, как возгонка,или сублимация.
Возьмем воду и будем понижать давление, температура плавления будет повышаться, а температура кипения понижаться. При этом возможно, что обе последние точки совпадут. Давление, при котором это происходит, называют иногда критическим. Приближенное вычисление для воды дает для критического давления 4,5 мм, а для температуры Т=0,007 [°С]. Следовательно, при таком давлении лед будет переходить прямо в пар. Строго говоря, мы имеем здесь дело с состоянием неустойчивого равновесия, и след[овательно], при таком давлении тело с одинаковой легкостью может быть в твердом, жидком и газообразном состоянии (Plank) [Planck]. Относительно льда проверка была произведена Carnelley’ем, хотя в противно [сть?] его мнению лед не может быть при этом нагрет выше температуры плавления. Другие тела уже при обыкновенной температуре и давлении обладают такими свойствами: так, йод, камфора и нафталин могут быть получены в жидком виде лишь при уменьшении давления, мышьяк и C2Cl6(Perchloraethan) — при повышении.
Такую точку можно бы назвать второю критический] точкой, но размягчение некоторых тел перед плавлением дает нам указание, что, быть может, возможна и третья критическая точка, средняя между твердым и жидким состоянием, т.е. когда удельные объемы твердого тела и жидкости будут равны.
По вычислению Планка, для воды третья крит[ическая] точка должна быть приблизительно при —120° и 15 ООО атм давления, но из рассматривания свойств термодинамической поверхности он заключает, что по крайней мере для воды существование такой точки является невозможным.
Считаю ответ удовлетворительным. Весьма удовлетворительно.
М. Авенариус Н. Шиллер М. Хандриков В. Ермаков М. Ващенко-Захарченко
ПРИЛОЖЕНИЕ 2 [60]
В физико-математический факультет
от профессора Н. Шиллера
Имею честь представить на одобрение факультета план предполагаемых занятий г. Надеждина во время его заграничной командировки, о представлении к каковой я ходатайствовал перед факультетом.
Прежде всего рекомендуется г. Надеждину сосредоточить свои занятия по возможности преимущественно при Берлинском университете, обладающем образцовою физическою лабораториею и первоклассными профессорами. Экспериментальные занятия г. Надеждина будут происходить в физическом институте университета, под руководством профессора фон Гельмгольца, причем рекомендуется предпочтительнее избрать специальную тему для экспериментального исследования, не останавливаясь на рядовых измерительных задачах, входящих в курс практических упражнений. Само собою, однако, разумеется, что г. Надеждин должен будет, в видах педагогических, ознакомиться с общим характером физических упражнений, введенных в Берлинском физическом институте, а также и с детальным устройством этого последнего.
Что касается до теоретической части изучаемой г. Надеждиным науки, то для усовершенствования в оной г-н Надеждин прослушает ряд курсов профессора Кирхгофа по механике, теории упругости, тепла, света и электричества и, кроме того, ознакомится с преподаванием экспериментальной физики профессора фон Гельмгольца. Желательно было бы, чтобы г. Надеждин, если у него найдется на то время, прослушал бы курс профессора Вейерштрасса, по крайней мере хотя об общей теории функций. Также ставится на вид г. Надеждину, что некоторые главы теоретической физики читаются в Берлинском университете докторами Кайзером и Ароном.
Буде обстоятельства не позволят г. Надеждину приступить тотчас же к занятиям в Берлине, то ему рекомендуется физический институт Страсбургского университета, состоящий в ведении профессора Кундта. Но желательно было бы, чтобы г. Надеждин не выбирал себе конечною целью пребывание при Страсбургском университете, а постарался бы воспользоваться советами и руководством профессора фон Гельмгольца.
Кроме вышесказанного, вниманию г. Надеждина рекомендуется физический институт в Граце, где он найдет превосходного руководителя в лице профессора Больцмана.
Отчеты г. Надеждина могут состоять в изложении хода его экспериментальных работ, описании посещаемых им физических лабораторий и в изложении избранных глав из прослушанных им лекций.
8 сентября 1885 г.
Подлинное подписал профессор Н. Шиллер.
С подлинным верно:
Ректор (подпись)
Принятые сокращения:
ААН – Архив Академии Наук СССР, Ленинградское отделение.
ВОФЭМ – Вестник опытной физики и элементарной математики.
ЖРФХО – Журнал Русского Физико-Химического Общества, часть физическая.
КГА – Киевский городской архив.
КОЕ – Записки Киевского общества естествоиспытателей.
КУИ– Киевскиеуниверситетскиеизвестия.
Beibl. – Beiblätter zu Wiedemanns Annalen der Physik und Chemie.
1. Жук К.Н. К вопросу о температуре абсолютного кипения жидкостей (Из рукописного сочинения студента А. Надеждина)// КУИ. Ч. неофиц. Отд. III. Февр. 1882. С. 1—6. - То же // ЖРФХО, Ч.физ. Отд. 1.1882. Т. 14, вып. 4. С. 157-161.
2. Надеждин А.И. К вопросу о температуре абсолютного кипения жидкостей // КУИ. Окт. 1882. С. 23-28. - То же // ЖРФХО. Отд. 1.1882. Т. 14. вып. 4. С. 536- 541.
3. Надеждин А.И. К вопросу о критической температуре изомеров и гомологических рядов II КУИ. Февр. 1883. С. 27-32. - То же // ЖРФХО. Отд. I 1883. Т. 15, вып. 2. С. 25-29.
4. Надеждин А.И. О некоторых новейших исследованиях, в связи с общим направлением современной физики: Речь, произнесенная на выпускном акте Киевской женской гимназии 15 июля 1883 года. Киев, 1883. 33 с.
5. Надеждин А.И. Несколько слов по поводу статьи г. Павлевского ”Uebег diekritischenTemperatureneinigerFlüssigkeiten// ЖРФХО. Отд. 1.1884. Т. 16, вып. 2. С. 74-75.
6. Надеждин А.И. О теплоемкости жидкостей // Там же. Вып. 4. С. 222-237.
7. Nadejdin A. I. Die spezifische Wärme der Flüssigkeiten und ihre Beziehung zu deren anderen physikalischen Eigenschaften // Exner’s Repertorium der Physik, 1884, Bd. 20, S.440-445. Реферат:Beibl. 1885, Bd. 9, S. 109-110.
8. Nadejdin A. I. La détermination de la température critique dans les tubes opaques// Bull. Imp. Acad. Sci. St. Petersburg, 1885, Т. 30. Р. 327-330. — Idem // Mélanges phys. et chim., 1885, Т. XII. Р. 299-304. - Рефераты: Веibl., 1885, Bd. 9, S. 721-723; Chemisches Zentralblatt, 1886, S.401-402.
9. Надеждин А.И. Определение критической температуры азотной кислоты, брома, йода и воды // КУИ. 1885. Июнь. С. 21-34.
10. Надеждин А.И. Этюды по сравнительной физике // Там же. Окт. С. 52-76; Нояб. С. 77-104; Дек. С. 105-140; 1886. Янв. С. 1-38; Февр. С. 39-74. - То же: Отдельное изд. Киев, 1886.163 с.
11. Надеждин А.И. Физические исследования/С предисловием М. П. Авенариуса и биографическим очерком. Киев, 1887. XII + 172 с.. В книгу включены работы [10] и [9]. Рецензии: ВОФЭМ, 1887, № 14, с. 38-39; Русская мысль, 1887, № 8, библиографический отдел, с. 494-496.
12. Nadejdin A. I. Über die Ausdehnung der Flüssigketen und den Übergang der Körper aus dem flüssigen in der gasförmigen Zustand // Exner’s Repertorium der Physik, 1887, Bd. 23, S. 617-649,685-718. Реферат: Chemisches Zentralblatt, 1888, S. 168.
13. Nadejdin A. I. Über die Spannkraft der gesättigten Dämpfe, Ibidem, S. 759-790.
14. Надеждин А.И. К вопросу о температуре абсолютного кипения жидкостей (Сообщение о работе Надеждина сделано К. Н. Жуком 24 апреля 1882 г.)// КОЕ, 1883. Т. 7, вып. 1, c. ХХХII-ХХХIII. (Здесь и далее до № 20 включительно – авторефераты сообщений в Киевском обществе естествоиспытателей. В скобках указаны даты докладов).
15. Надеждин А.И. О теплоемкости жидкостей (3 марта 1884 г.) //КОЕ, 1884. Т. 7, вып. 2, с. ХСIХ-С.
16. Надеждин А.И. Об отношении между теплоемкостью и теплом испарения жидкостей (28 апреля 1884 г.) // КОЕ, 1886. Т. 8, вып. 1, с. II—III.
17. Надеждин А.И. О способе определения критической температуры в непрозрачных трубках (12 января 1885 г.) // Там же. с. XVII—XVIII.
18. Надеждин А.И. О критической температуре (18 мая 1885 г.) // Там же, с. LI.
19. Надеждин А.И. О деполяризующем влиянии марганцовокислого калия (18 мая 1885 г.) //Там же,c. L-LI.
20. Надеждин А.И. Об упругости насыщенных паров при высоких температурах (21 декабря 1885 г.) // Там же, c. LXXXI-LXXXIII.
21. Б[укреев Б.Я.]. Биографический очерк // Надеждин А.И. Физические исследования. Киев, 1887, с. VII-XII.
22. Шпачинский Э.К. Александр Иванович Надеждин. Некролог // ВОФЭМ. 1886. № 1. с. 16-18.
23. Дело канцелярского совета Ун-та Св. Владимира ”0 рекомендовании Министерству Народного Просвещения стипендиата Надеждина”. 1882 // КГА, Ф. 16. Оп. 321. Д. 177.47 л.
24. О полукурсовых испытаниях студентов, 1879 // Там же. Оп. 318. Д. 108. Л. 21, 31.
25. Шпачинский Э.К. Михаил Петрович Авенариус. Некролог // ВОФЭМ, 1895. № 3 (219), с. 49-55.
26. Косоногов И.И. Речь у гроба М.П. Авенариуса // ААН. Ф. 765. Оп. 1. № 45. Л. 13-15.
27. Столетов А.Г. М.П. Авенариус // Собр. соч. М. Л.: Гостехтеориздат, 1941. Т. 2, с. 417-435.
28. Историко-статистические записки об ученых и учебно-вспомогательных учреждениях имп. Университета Св. Владимира (1834-1884). Киев, 1884.416 с.
29. Розенберг М.И. Из истории учения о критическом состоянии вещества (по работам Киевской школы физиков второй половины XIX столетия) // Физика в школе, 1950, №3, с. 20-27.
30. Якобсон И.Я. Проблема критического состояния веществ в трудах физиков Киевского университета (1870-1886) //Природа, 1951, № 2, с. 77-84.
31. Гольдман А.Г. М.П. Авенариус и Киевская школа экспериментальной физики // УФН, 1951. Т. 44, вып. 4, с. 586-609.
32. Сивцев Д.М. Роль русских ученых в изучении критического состояния тел во второй половине XIX века: Диссертация… канд. физ.-мат. наук. М. МГУ, 1952.
33. Русаков В.П. Киевский физик М.П. Авенариус // Тр. ИИЕТ. 1955. Вып. 5, с. 180— 215.
34. Центр, гос. истор. архив Украины (Киев) (ЦГИАУ). Ф. 707. Оп. 39. Д. 37 (1873).
35. Страус О.Э. Памяти В.И. Зайончевского//Физ. обозрение. 1909. Т. 10, № 4. с. 202-204.
36. Зайончевский В.И. Определение упругости паров некоторых жидкостей при высоких температурах // КУИ. Ч. неофиц. Отд. III. 1878. № 4. С. 21-49, № 8. С. 29- 39. — Реферат: Beibl., 1897. Bd. 3, S. 741-743.
37. Зайончевский В.И. Несколько слов по поводу "Заметки о критическом состоянии тел” проф. Столетова // ЖРФХО. 1882. Т. 14, вып. 7, c. 386-388.
38. Косоногов И.И. Памяти К.Н. Жука // ААН. Ф. 765. Оп. 1. Д. 50.
39. Жук К.Н. Объем жидкости как функция температуры при постоянном давлении// ЖРФХО. Отд. I. 1880. Т. 12, вып. 1/2. с. 66; 1881. Т. 13, вып. 5. с. 239-241; вып. 9. с. 411-413; 1884. Т. 16, вып. 6. с. 304-306.
40. Жук К.Н. К вопросу о расширении жидкостей // КУИ. 1884. № 9. с. 11-18; ЖРФХО. Отд. I. 1885. Т. 17, вып. 1. с. 13-19.
41. Страус О.Э. О критических температурах некоторых смесей // ЖРФХО. Отд. I. 1880. Т. 12, вып. 7. С. 207-218, 233. - Реферат: Beibl., 1882, Bd.. 6, S. 282.
42. Страус О.Э. О критической температуре и критическом давлении воды // ЖРФХО. Отд. I. 1881. Т. 13, вып. 5. С. 270; 1882. Т. 14, вып. 9. С. 510-517. -Реферат: Beibl., 1883, Bd. 7, S. 1676.
43. КГА. Ф. 16. Оп. 319 (1880), д. 184. л. 6-8.
44. О темах на сочинения для соискания наград медалями (1879) // КГА, Ф. 16, Оп. 318. д. 165. л. 9.
45. Magnus G. Über Ausdehnung der atmosphärischen Luft in höheren Temperaturen, Poggendorffs Ann. Phys. Chem. 1842, Bd. 57, S. 177-199.
46. Голъдгаммер Д.А .Памяти профессора А.Г. Столетова // Изв. физ.-мат. о-ва при Казанском ун-те. 1897. Т. 7, № 1. С. 39-54.
47. Жук К.Н. Объем жидкости как функция температуры при постоянном давлении. // ЖРФХО, 1884. Т. 16, вып. 6, с. 304-306. -Реферат: Beibl., 1884, Bd.. 8, S. 808-809.
48. КГА. Ф. 16. Оп. 319 (1880), д. 184. л. 32.
49. КГА. Ф. 16. Оп. 321 (1882), д. 131. л. 3-4, 20, 31.
50. КГА. Ф. 16. Оп. 472 (1882). Д. 239. Л. 4.
51. Там же. Д. 240. Л. 6.
52. Planck M. Verdampfen, Schmelzen und Sublimiren. // Ann. Phys. Chem. 1882, Bd.15, S. 446-475.
53. Дело о защшцении диссертации магистром Александром Надеждиным (1886) // КГА. Ф. 16. Оп. 325. д. 67.
54. О зачислении некоторых молодых людей в стипендиаты // Там же. Оп. 321 (1882). Д. 117. Л. 146, 195.
55. Рождественский С.В. Исторический обзор деятельности министерства народного просвещения, 1802—1902. СПб., 1902. 785 с.
56. Протоколы собраний Киевского общества естествоиспытателей, 30 янв. и 12февр. 1883 г. // КОЕ. 1883. Т. 7, вып. 1, c. ХХVII-ХХVII, LI.
57. Устав Киевского общества естествоиспытателей // КУИ. Ч. офиц., 1869, № 5, c. 1-6.
58. КГА. Ф. 16. Оп. 323 (1884). д. 12. л. 68.
59. Центр, гос. ист. арх. в Ленинграде (ЦГИАЛ). Ф. 733. Оп. 149 (1885). д. 777. л. 400-402 об.
60. Там же. Л. 399, 399 об.
61. Шпачинский Э.К. Письмо к Б.Б. Голицыну от 30 декабря 1888 г. // ААН. Ф. 69. On. 1. д. 33, л. 1, 1об.
62. Голицын Б.Б. О газообразном и жидком состоянии вещества // ВОФЭМ. 1889. VI сем. с. 85-97, 133-144, 177-186, 221-231; VII сем. с. 21-31, 62-72, 141- 156; 1890. VIII сем. с. 21-28, 41-51.
63. Kamerlingh-Onnes Н. Allgemeine Theorie der Flüssigkeiten // Beibl. 1881, Bd. 5, S. 718-726.
64. Гезехус H.A. Исторический очерк десятилетней деятельности Физического общества // ЖРФХО. 1882. Т. 14, вып. 9, c. 518-535.
65. Столетов А.Г. Гельмгольц и современная физика (1894) // Собр. соч. М.: Гостехтеориздат, 1941. Т. 2, c. 307-340.
66. Столетов А.Г. Г.Р. Кирхгоф (1873) // Там же. c. 31-52.
67. Dellingshausen N. Grundzüge einer Vibrationstheorie der Natur. Leipzig: Hartmann, 1872. IX + 405 S.
68. Dellingshausen N. Grundzüge der kinetischen Naturlehre. Heidelberg: Winter, 1898. VIII+520 S.
69. Dellingshausen N. Beitrage zur mechanischen Wärmetheorie. Heidelberg: Winter, 1874. II+102 S.
70. Stallo L.B. The concepts and theories of modern physics. Cambridge (Mass.): Harvard Univ. press, 1960. XXIX+325 p.
71 . Кипнис А.Я., Явелов Б.Е. Иоганнес Дидерик Ван-дер-Ваальс. Л.: Наука, 1985. 310 с.
72. Pictet R. Mémoire sur la liquéfaction de l’oxygène, la liquéfaction et la solidifaction de l’hydrogéne et sur les théories des changements d’état des corps // Arch. sci. phys. et natur. Genève, 1878. T. 61. p. 16-108.
73. Фонберг [Г.М]. О необходимости наук для успеха искусств и ремесел // Журн. Министерства народного просвещения. Отд. II. 1853. Т. 80, с. 72-100.
74. Столетов А.Г. О критическом состоянии тел (статья вторая) // Тр. Отд. физ. наук. О-ва любителей естествознания. 1892, Т. 5, вып. 1, с. 1 — 15.
75. Стенли Г. Фазовые переходы и критические явления. М.: Мир, 1973. 419 с.
76. Эндрюс Т. О непрерывности газообразного и жидкого состояний вещества. М. Л.: Гостехтеориздат, 1933. 120 с.
77. Avenarius М. Über innere latente Wärme // Ann. phys. Chem. 1874. Bd. 151, S. 303— 316.
78. Altschul M. Über die kritischen Grössen einiger organischen Verbindungen // Ztschr. physik. Chem. 1893. Bd. 11, S. 577-597.
79. Wesendonck K. Über den kritischen Zustand // Ibid. 1894. Bd. 15, S. 262-266.
80. Kamerlingh-Onnes H., Keesom W.H. Die Zustandsgleichung (1911)// Enc. Math. Wiss. Leipzig, 1921. Bd. 5, T. 1. S. 615—956. — Idem // Leiden Communications 1912. Suppl. N 23. 352 S.
81. Шпачинский Э. Новый прием г. Надеждина для определения критической температуры // Журн. элементар. математики. 1885. Т. 1, № 13. С. 241-244.
82. Ostwald W. Lehrbuch der allgemeinen Chemie. 2. Aufl. Leipzig: Engelmann, 1891. Bd. 1. S. 243
83. Хвольсон О.Д. Курс физики. Берлин, 1923. Т. 3. c. 648.
84. Jellinek К. Lehrbuch der physikalischen Chemie. 2. Aufl. Stuttgart: Enke, 1928. Bd. 1. S. 602.
85. Heilborn E. Zusammenstellung der bisher ermittelten kritischen Daten der Flüssigkeiten // Ztschr. physik. Chem. 1891. Bd. 7, S. 601-613.
86. Landolt-Bornstein. Zahlenwerte und Funktionen aus Naturwissenschaften und Technik. Berlin: Springer, 1971. Bd. 2. T. 1. Tab. 211161.
87. Критические величины и константы Ван-дер-Ваальса // Справочник химика. 3-еизд. Л.: Химия, 1971. Т. 1. С. 731-736.
88. Avenarius М. Über die Ursachen welche die kritische Temperatur bedingen // Bull. Imp. Acad. Sci. St. Petersburg. 1876. T. 22, N 3. P. 378-389.
89. Van der Waals I.B. Die Continuitat des gasförmigen und flüssigen Zustandes. Leipzig: Barth, 1881. VIII+168 S.
90. Столетов А.Г. Заметки о критическом состоянии тел // ЖРФХО. Отд. 1. 1882. Т. 14, вып. 5, c. 167-175.
91. Авенариус М.П. Критическое состояние тел // Журн. элементар. математики. 1884. Т. 1, № 5, c. 89-100.
92. Столетов А.Г. Письма к В.А. Михельсону от 21 янв. и 24 сент. 1892 г. // ААН. Ф. 328. Оп. 2. № 61, л. 54., 63 об.
93. Столетов А.Г. О критическом состоянии тел. Статьи третья и четвертая / ЖРФХО. Отд. I. 1893. Т. 25, вып. 9. с. 303-326; 1894. Т. 26, вып. 1. с. 26-30.
94. Levelt Sengers J.M.H. Liquidons and gasons: controversies about continuity of states // Physica A. 1979. vol. 98. p. 363-402.
95. Карапетъянц M.X., Чэм Гуаг-юе. Температура кипения и давление насыщенного пара углеводородов. М.: Гостоптехиздат, 1961. 242 с.
96. Вукалович М.П., Новиков И.И. Техническая термодинамика. М.: Госэнергоиздат, 1952. 245 с.
97. Бадылькес И.С. Рабочие вещества холодильных машин. М.: Пищепромиздат, 1952. 74 с.
98. Бадылькес И.С. Термодинамическое подобие рабочих веществ и процессов холодильных машин. М.: Госторгиздат, 1960. 64 с.
99. Новиков И.И. Термодинамика. М.: Машиностроение, 1984. 592 с.
100. Путилов К.А. Термодинамика: Наука, 1971. 376 с.
101. Филиппов Л.П. Подобие свойств веществ. М.: Изд-во МГУ, 1978. 256 с.
102. Филиппов Л.П. Прогнозирование теплофизических свойств жидкостей и газов. М.: Энергоатомиздат, 1988. 168 с.
103. Gibbs J.W. The collected Works. N.Y. etc.: Longmans, 1928. Vol. 1.
104. De Heen P. Essai de physique comparée. Bruxelles, 1883. 167 p. (Mém. couronnés et autres mém. publ. Acad. Roy. Belg., T. 36).
105. Менделеев Д.И. Замечания по поводу работы Эндрюса над сжимаемостью углекислоты (1870) // Соч. Л.; М.: Изд-во АН СССР, 1947. Т. 5. С. 107-112.
106. Pawlewski Br. Über die kritischen Temperaturen einiger Flüssigkeiten // Ber. Dt. chem. Ges. 1883. Bd. 16. S. 2633-2636.
107. Vincent C., Chappuis J. Sur les temperatures et les pressions critiques de quelques vapeurs// C. r. Acad. sci. 1885. T. 101. p. 427-429.
108. Булатов А. К вопросу о критической температуре //ЖРФХО. 1899. Т. 31, вып. 4, c. 69-81.
109. Библиотека Менделеева // Научный Архив-музей Д.И. Менделеева (Ленинград). № 150/4.
110. Каталог книг Д.И. Менделеева (Тетрадь по библиотеке), 1897 // Там же.
111. Guldberg С.М. Über die Gesetz der Molekularvolumina und der Siedepunkt // Ztschr. physik. Chem. 1890. Bd. 5. S. 374-382.
112 Meslin G. Sur l’equation de Van-der-Waals et la démonstration du théoreme des états correspondents // C. r. Acad. sci. 1893. T. 116. p. 135 -136.
113. Meyer K. Über korrespondierende Zustande der Stoffe // Ztschr. physik. Chem. 1900. Bd. 32. S. 1-38; 1910. Bd. 71. S. 325-336.
114. Эренфест-Афанасъева ТА. К теории соответствующих состояний //ЖРФХО. Отд.II, 1914. Т.46, вып. 8. С. 336-343.
115. Young S. On the generalisations of Van der Waals regarding corresponding temperatu¬res, pressures and volumes // Phil. Mag. 1892. Vol. 33. P. 153—185; 1894. Vol. 37. P. 1-8.
116. Partington J.R. An advanced treatise on physical chemistry. L.: Longmans, 1949. Vol. 1. P. 688-702.
117. Раковский А.В. Предисловие // Ван-дер-Ваальс И.Д., Констамм Ф. Курс термостатики. М., Л.: ОНТИ, 1936. Т. 1. c. 1-7.
